Enlace iónico
Cuando un elemento muy electropositivo (un metal de la parte izquierda de la tabla periódica) se une a un elemento muy electronegativo (un no metal de la parte derecha de la tabla periódica) se produce una unión mediante enlace iónico. Matemáticamente, este tipo de enlaces ocurre cuando la diferencia de electronegatividades entre los átomos es mayor o igual que 1,7.

El metal pierde uno o varios electrones, convirtiéndose en un catión. La energía necesaria para este proceso es el potencial de ionización. El no metal captura uno o varios electrones y se convierte en un anión, la energía que se libera en este caso es la afinidad electrónica. Puesto que los iones se unen por fuerzas electrostáticas, no forman una molécula sino un cristal: Es la energía procedente de la unión de los iones la que proporciona estabilidad al enlace iónico.
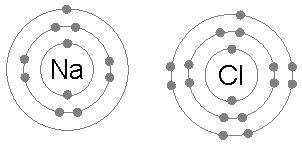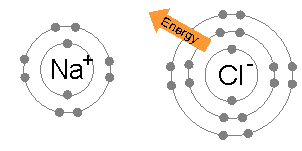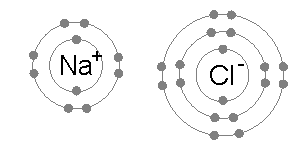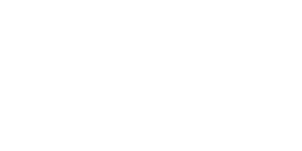
Átomo de sodio y de cloro formado un enlace iónico, indicando la transferencia de energía. CC 3.0 by: Tra.
Las sustancias iónicas forman redes cristalinas por lo que, a temperatura ambiente, serán sólidos con puntos de fusión y ebullición elevados. Serán duros puesto que tanto rayarlas, como fundirlas o evaporarlas, supone romper la fuerza electrostática que une los iones, pero relativamente frágiles, porque un golpe desplazará los iones y ocasionará que prevalezcan las fuerzas repulsivas, rompiendo el cristal.
En disolventes polares, como el agua, se disolverán, ya que las moléculas de agua son dipolos, tienen una parte positiva y otra negativa, con lo que rodearán los iones de la red cristalina y los atraerán al interior del líquido, rompiendo la atracción entre los cationes y aniones que forman el cristal. El proceso por el que los dipolos del agua rodean los iones se llama solvatación.
Las sustancias iónicas son aislantes, no conducen la electricidad porque carecen de cargas eléctricas móviles. Sin embargo, cuando están disueltas o fundidas, puesto que los iones se pueden mover con libertad en el líquido, sí conducen la electricidad: son buenos conductores.